 作者
作者  通讯作者
通讯作者
基因组学与应用生物学, 2011 年, 第 30 卷, 第 3 篇 doi: 10.5376/gab.cn.2011.30.0003
收稿日期: 2011年01月05日 接受日期: 2011年01月25日 发表日期: 2011年01月28日
引用格式(中文):
濮仕颖, 2011, 黄单胞菌基因组6~8 kb克隆库构建初探,基因组学与应用生物学(online), Vol.30 No.3 pp.1011-1015 (doi: 10.5376/gab.cn.2011.30.0003)
引用格式(英文):
Pu Shiying., 2011, Establishment of 6~8 kb genomic clone library from Xanthmonas, Jiyinzuxue Yu Yingyong Shengwuxue (Genomics and Applied Biology), Vol.30 No.3 pp.1011-1015 (doi: 10.5376/gab.cn.2011.30.0003)
黄单胞菌能引起植物白叶枯病。从已测得的部分黄单胞菌XOO基因组序列来看,发现其中含有较多的重复序列。为了能更准确地获得黄单胞菌XOO全基因组序列,本文对传统的鸟枪法建库方法中电泳回收DNA这一实验步骤进行了适当的修改,并成功地构建了插入片段大小在6~8 kb区域的鸟枪法克隆文库,建立了黄单胞菌XOO 6~8 kb克隆库构建方法。本研究结果将为今后黄单胞菌XOO全基因组序列中的重复序列准确地拼接、定位及其基因组结构的有效研究提供依据及支持,并进一步阐明黄单胞菌XOO的致病机理奠定基础。
黄单胞菌(Xanthmona)是一种大小为1.0~2.7 μm×0.5~1.0 μm,直杆状细菌,单生,端生鞭毛运动,专性好氧,极生或亚极生,长约8.7 μm,直径为30 nm,属于革兰氏阴性菌,没有芽孢和荚膜,在菌体外有粘质的胞外多糖。在人工培养基上菌落呈蜜黄色,会产生一种非水溶性的黄色色素,呼吸型代谢,不同地区的菌株对植物的侵染能力不同。自然条件下,黄单胞菌可侵染栽培稻、野生稻、李氏禾和茭白等禾本科植物。17~33℃为黄单胞菌的生长温限,其中最适的温度范围为25~30℃,也能存活于最低5℃最高40℃的温度中,最适宜的pH值范围为pH 6.5~7.0 (张华, 2004)。黄单胞菌能引起白叶枯病。植物在整个生育期里都有可能受到侵染(孙其红等, 2004)。在苗期、分蘖期这两个时期最容易受到伤害。而且植物的各个器官均有可能染病,其中叶片部分最易染病。所以研究黄单胞菌基因组结构及特征,便显得尤为重要了。
近年来随着新型DNA测序仪,例如454、Solexa和SOLiD等的出现和发展,使得测序成本和时间大大地降低,加速了基因组的全面分析的进程。但目前的454、Solexa和SOLiD测序仪测出的序列长度相比第一代利用DNA双脱氧测序技术的3730xl (ABI公司)短得多(张闻等, 2009; 严安和熊慧, 2010),3730xl测出的序列平均长度800 bp以上,而454、Solexa和SOLiD测序仪中能测出的最长序列的454测序仪测出的序列平均长度400 bp。众所周知,在一些生物基因组中存在大量重复序列,它们对生物体的基因表达和染色体的生理代谢有着重要的意义。目前对基因组DNA序列的测定主要是使用鸟枪法进行测序。鸟枪法是将基因组随机打断(一般打断后选取片段大小在2~3 kb区域的片段进行文库构建),然后利用计算机进行序列拼接。那么如果测出的序列长度越长,相对的序列的特异性也越高,也越有利于序列正确拼接(贾凌等, 2010)。
对于全基因组测序,我们也可以建立BAC、fosmid和cosmid等文库后进行测序拼接,但这几种文库的构建相对于2~3 kb的文库构建复杂得多,所以本试验参考脉冲场凝胶电泳技术,在构建常规的1.6~4 kb的鸟枪法文库的基础上,对其电泳部分的试验步骤进行改进,初步建立了黄单胞菌XOO 6~8 kb克隆库构建方法,减少后续的计算机处理序列,序列拼接以及补洞阶段的难度,为进一步阐明黄单胞菌XOO的致病机理和基因组结构研究奠定基础。
1 结果与分析
1.1改良方法构建的黄单胞菌6~8 kb鸟枪法文库的克隆质粒抽提及检测
我们挑取96个采用在电泳部分的试验步骤进行改进后的方法构建的黄单胞菌XOO的插入片段大小在6~8 kb左右的克隆文库的克隆子,经质粒抽提后电泳检测其片段的插入情况来看(图1),可以看到96个克隆子中有93个克隆子的有较大片段的插入,比例达到近97%。
 图1 用改进后方法构建的黄单胞菌XOO 6~8 kb文库的亚克隆检测图 |
1.2常规方法构建的黄单胞菌6~8 kb鸟枪法文库的克隆质粒抽提及检测
我们挑取96个在电泳部分采用常规的两次电泳跑胶回收纯化方法构建的黄单胞菌XOO的6~8 kb克隆文库的克隆子,经质粒抽提后电泳检测其片段的插入情况来看(图2),可以看到96个克隆子中有48个克隆子的有较大片段的插入,比例为50%。
 图2采用在电泳部分的实验步骤进行未改进的方法构建的黄单胞菌XOO 6~8 kb文库的96个克隆检测图 |
1.3亚克隆质粒测序
将有插入片段的质粒用引物SL1、SR2 (CloneSmart® Cloning Kits, Lucigen公司)用3730xl测序仪(ABI公司)进行测序。改良方法构建的黄单胞菌6~8 kb鸟枪法文库的克隆子测得序列平均长度723 bp,93个质粒成功93个;常规方法构建的黄单胞菌6~8 kb鸟枪法文库的克隆子测得序列平均长度745 bp,48个质粒成功48个。
1.4结果比较
从试验结果来看,改良方法构建的黄单胞菌6~8 kb鸟枪法文库相比常规方法构建的黄单胞菌6~8 kb鸟枪法文库插入率高,在96个随机挑取的克隆子中大片段的插入个数从48个提高到93个(图3),比例从50%提高到97% (图4)。也能使用3730xl测序仪进行测序,且测得的序列的平均长度和成功率并没有被影响。所以用此改良方法对黄单胞菌基因组DNA构建插入片段为6~8 kb的平端克隆文库的方法是可行的。
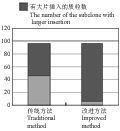 图3改进前后96个克隆子中大片段插入的克隆子数 |
.png) 图4改进前后96个克隆子中大片段插入的克隆子所占的比例 |
2讨论
琼脂糖凝胶电泳是用琼脂糖作支持介质的一种电泳方法,它兼有“分子筛”和“电泳”的双重作用。琼脂糖凝胶具有网络结构,物质分子通过时会受到阻力,大分子物质在涌动时受到的阻力大,因此在凝胶电泳中,带电颗粒的分离不仅取决于净电荷的性质和数量,而且还取决于分子大小。但琼脂糖凝胶电泳不可能完全将不同大小的DNA片段分离开来,在通过切胶回收下的6~8 kb片段中会含有几百bp的小片段,这些片段在和载体通过连接酶进行平端连接的过程中小片段会优先和载体进行连接,造成大片段的插入率低。那么降低6~8 kb片段中几百bp小片段的含量就能减少小片段的插入,提高6~8 kb片段的插入率。在第二次跑胶完成后改变电极方向再次进行电泳,相当于增加一次电泳过程,从而减少几百bp小片段的含量。
在对黄单胞菌基因组DNA进行全基因组测序最初,我们构建了1.6~4 kb的文库。1.6~4 kb的文库大部分插入片段的大小在2~2.5 kb,对其测序后发现黄单胞菌基因组DNA序列有较多的重复序列,使用PhredPhrap软件进行拼接后发现因为重复序列的关系很多序列在拼装时拼接位置错误,且因为有些重复区域比较大,无法准确判断序列的正确拼接位置,无法校正,所以构建稍大一点的随机文库(6~8 kb)可以改善这一情况,帮助后期的序列拼装。6~8 kb随机文库相比1.6~4 kb随机文库的优点有:6~8 kb随机文库的插入片段比常规的1.6~4 kb随机文库插入片段长,在基因组上跨的区域大些,能做框架使用,对于后期的gap-closing有更大的帮助;6~8 kb随机文库的每个克隆子比常规的1.6~4 kb随机文库每个克隆子所含的基因信息多且完整,可以为今后的蛋白表达和基因功能分析等提供更多克隆子。
我们之所以选用超声打断DNA和载体进行平端连接的方法构建随机文库,而不使用限制性酶切基因组DNA得到6~8 kb片段,是因为限制性内切酶有一定的选择性,所以从随机性来说,采用超声随机打断的方法得到6~8 kb片段其随机性更好,得到的片段能覆盖到全基因组的区域更大。
fosmid、cosmid和BAC这些文库构建时需要用到脉冲场电泳仪。因为脉冲场电泳仪购价比较高,很多实验室不具备此设备,而且相对于fosmid、cosmid和BAC文库,6~8 kb的片段大小更容易获得,且文库构建方法较简单,容易操作。同时从对质粒测序上来看,含6~8 kb插入片段的质粒相比fosmid、cosmid和BAC这些插入片段在30 kb以上的质粒,测序的成功率高,测得的片段长度也长。
3材料与方法
3.1供试材料
黄单胞菌XOO DNA为本室保存。
3.2主要试剂
细菌基因组DNA小量制备试剂盒(AxyGen公司),DNATerminator® End Repair Kit (Lucigen公司),CloneSmart LCKan Blunt Cloning Kit (Lucigen公司),QIAquick Gel extraction kit (Qiagen公司),LE Agarose (Promega公司)。
3.3主要仪器
超声波粉碎仪(550 Sonic Dismembrator, Fisher Scientific公司),电泳仪(EPS-300, Tanon公司),紫外成像仪(FR-200, 复日科技公司),电转仪及电转杯(Bio Rad公司),恒温培养箱(GRP-9610, 上海森信实验仪器有限公司)。
3.4黄单胞菌XOO DNA纯化与打断
将黄单胞菌XOO DNA用细菌基因组DNA小量制备试剂盒(AxyGen公司)按操作手册纯化DNA。取纯化好的约20 ug DNA超声打断后使用1%琼脂糖进行凝胶电泳检测,确定超声后DNA的片段主要的集中在6~8 kb区域。
3.5 DNA片段补平及主带片段回收纯化
将超声打断的DNA溶液在1%的琼脂糖凝胶(LE Agarose, Promega公司)上,于1×TAE电泳缓冲液中,在3.5 V/cm的电场强度电泳3 h。将Marker切下用EB染色,对应Marker切下主带的片断,根据操作手册用QIAquick Gel Extraction Kit回收。将回收后的片断按DNATerminator® End Repair Kit (Lucigen公司)操作步骤进行补平。再将补平后的DNA溶液在1%的琼脂糖凝胶(LE Agarose, Promega公司)上,于1×TAE电泳缓冲液中,在4 V/cm的电场强度电泳10 h,每4 h换一次缓冲液。再改变电极方向再电泳5 h。切下Marker区域,用EB染色后,对应切下6~8 kb。用QIAquick Gel extraction kit (Qiagen公司)回收主带位置的DNA片段。回收后的主带片段按CloneSmart LCKan Blunt Cloning Kit (Lucigen公司)操作步骤进行。
3.6主带片段与载体pSMART连接
回收后的主带片段按CloneSmart LCKan Blunt Cloning Kit (Lucigen公司)操作步骤进行。
3.7 DNA重组子转化及筛选
取1 uL连接液电转,按E. cloni®10G ELITE DUOs Electrocompentent Cell (Lucigen公司)操作步骤进行。取50 uL、150 uL电转后的培养液均匀涂布在Kana抗性的LB培养平板上(Kana终浓度25 ug/mL),在37℃,静置,培养过夜。
3.8 DNA重组子的质粒抽提、电泳检测、测序
在平板上挑取单个白色菌落,并接种于LB培养液中(Kana终浓度50 ug/mL),在37℃,250 r/min,摇床培养17.5 h后用碱裂解法抽提质粒。将抽提出的质粒在1%的琼脂糖凝胶上,于1×TAE电泳缓冲液中,在5 V/cm的电场强度电泳1 h后通过紫外成像仪进行拍照检测。将有大的插入片段的质粒用SL1、SR2引物(Lucigen公司)进行测序。
致谢
在整个试验过程以及最终成稿期间,感谢国家人类基因组南方研究中心王升跃教授的指导和测序部各位同仁的帮助,感谢同济大学生命科学院郭占云教授和汪世龙教授的帮助和指导。
参考文献
Jia L., Zhao A.C., Ma S.Y and He N.J., 2010, Determination of an effective method to sequence——Directional determination, Canxue Tongxun (Newsletter of Sericultural Science), 30(1): 19-25 (贾凌, 赵爱春, 马三垣, 何宁佳, 2010, 测定重复序列的一种有效方法——定向删除法, 蚕学通讯, 30(1): 19-25)
Sun Q.H., 2004, Pathogenicity of Xanthomonas oryzae pv. oryzae functional genomics analysis, Dissertation for Ph.D., Institute Microbiology Chinese Academy of Sciences, Supervisor: Fang R.X., and He C.Z., pp.1-3 (孙其红, 2004, 水稻白叶枯菌(Xanthomonas oryzae pv. oryzae)致病性的功能基因组学分析, 博士学位论文, 中国科学院微生物研究所, 导师: 方荣祥, 何朝族, pp.1-3)
Yan A., and Xiong H., 2010, Application of sequencing in clinical, Guangdong Yixue (Guangdong Medical Journal), 31(3): 279-280 (严安, 熊慧, 2010, 测序技术在临床诊疗中的应用, 广东医学, 31(3): 279-280)
Zhang H., 2004, Specific molecular diagnosis of Xanthomonas oryzae pv. Oryzae and Xanthomonas oryzae pv. oryzicola, Thesis for M.S., Nanjing Agricultural University, Supervisor: Liu F.Q., and Hu B.S., pp.1-3 (张华, 2004, 水稻白叶枯病菌和细菌性条斑病菌的分子检测技术研究, 硕士学位论文, 南京农业大学, 导师: 刘凤权, 胡白石, pp.1-3)